Архивы за 13.09.2015
СТЕКЛО И ДРУГИЕ МАТЕРИАЛЫ ИЗ МИНЕРАЛЬНЫХ РАСПЛАВОВ
Для получения минеральных расплавов и изделий из них применяют сырьевые материалы, температура плавления которых не превышает I 400… 1 500 °С. Таких исходных продуктов существует всего три вида: стеклянная шихта, горные породы и шлаки (металлургические и топливные). Один и тот же минеральный расплав в зависимости от скорости охлаждения и ряда других условий может затвердевать в аморфном (стеклообразном) или кристаллическом состоянии. Поэтому материалы, получаемые из расплавов, по структуре (а следовательно, и по свойствам) подразделяются на две группы: стеклообразные (СОМ) и стеклокристаллические (СКМ), или ситаллы[2]. К первым относятся стекло, каменное литье и шлаковое литье; ко вторым — стеклоситаллы, получаемые из специальных по составу стекол, петроситаллы, изготавливаемые из горных пород, и шлакоситаллы — продукты переработки шлаков. Стеклообразные материалы могут быть плотными (листовое стекло), ячеистыми (пеностекло) и волокнистыми (стекловата, каменная вата, шлаковата).
Защита металлов от коррозии
Коррозионное разрушение металлов обусловлено протеканием окислительно-восстановительных реакций в результате химического или электрохимического взаимодействия их с окружающей средой.
Химическая коррозия протекает при взаимодействии металлов с газами (02, S02 и др.) и неэлектропроводными жидкостями (нефтепродуктами, спиртом и т. д.).
Электрохимическая коррозия протекает в электропроводящих водных растворах и состоит из двух процессов: анодного — растворения одних участков металла; катодного — отложения металла на других участках. Интенсивность этих процессов тем выше, чем выше неоднородность металла, обусловленная примесями и включениями, границами зерен кристаллитов, структурной гетерогенностью, пористостью металлических и неметаллических поверхностных пленок, местными внутренними напряжениями, повреждениями поверхности и т. д.
Способы защиты металла от коррозии разнообразны.
Защита легированием осуществляется, например, при получении нержавеющих сталей.
Эффективна защита окисными пленками, которые получают травлением металла в сильных окислителях (оксидирование) или анодной обработкой в окислительных средах (анодирование).
Защита металлическими (катодными) покрытиями, электродный потенциал которых выше, чем у защищаемого металла (например, у омедненной стали), эффективна только до тех пор, пока они обеспечивают барьер между сталью и средой. При повреждении покрытия происходит электрохимическое растворение стали, причем более быстрое, чем было бы при отсутствии покрытия. В отличие от этого анодные металлические покрытия, такие как цинковые по стали, являясь более электроотрицательными, защищают основной металл, который в их присутствии работает как катод и поэтому сохраняется практически без изменения до тех пор, пока не растворится цинк.
Протекторная защита заключатся в том, что в коррозионной среде на определенном расстоянии от предохраняемой стальной конструкции размещают цинковые протекторы-аноды, на которые переносится процесс коррозии.
Катодную защиту применяют для магистральных трубопроводов, морских нефтепромысловых и других сооружений. Она заключается в том, что защищаемую конструкцию подсоединяют к отрицательному полюсу постоянно действующего источника тока и, таким образом, смещают потенциал стали, делая ее катодом по отношению к какому-либо протектору (обычно стальному лому), подсоединяемому к положительному полюсу источника тока и выполняющему функцию растворяющегося анода.
Защита неметаллическими покрытиями осуществляется нанесением на металл лакокрасочных материалов (это наиболее дешевый вид защиты).
Цветные металлы и сплавы
Из цветных металлов наибольшее применение в строительстве получили сплавы алюминия, применяемые в качестве конструкционного материала. Сплавы меди и титана употребляются главным образом для запорно-регулировочной арматуры, водопроводно-отопительных и электротехнических систем зданий и сооружений.
Алюминий и его сплавы. Алюминий — металл серебристо-белого цвета плотностью 2 700 кг/м3, с температурой плавления 658 °С. Чистый алюминий вследствие малой прочности в строительных конструкциях применяется редко. Применение находят его сплавы.
Сплавы алюминия характеризуются прочностью при растяжении Rp = 100…700 МПа и относительным удлинением 8 = 6…22 %. Модуль упругости алюминиевых сплавов почти в 3 раза ниже, чем у стали (0,7- 105 МПа). Марки алюминиевых сплавов состоят из букв и цифр, характеризующих состав сплава. Алюминиевые сплавы подразделяются на литейные и деформируемые (обрабатываемые давлением).
Литейные сплавы вследствие их низкой пластичности применяются в строительстве только для опорных частей конструкций (сплав АЛ-8).
Деформируемые сплавы применяются для производства листов, прессованных профилей, труб и прутков, а также для изготовления деталей ковкой и штамповкой. Их механические свойства повышают легированием (элементами Mg, Mn, Си, Si, Al, Zn), пластическим деформированием (нагартовкой) и закалкой с последующим старением при комнатной или повышенной температуре.
Деформируемые сплавы подразделяются на термически упрочняемые и неупрочняемые. К термически упрочняемым относятся:
1) авиаль (Al-Mg-Si) (АД31, АДЗЗ, АД35, АВ);
2) дюралюмин (Al — Си — Mg) (Д1, Д16);
3) высокопрочные сплавы на основе Al — Zn — Mg — (Си) (В92, В95);
4) ковочные жаропрочные сплавы (Al — Mg — Si — Си) (АК6, АК8).
К термически неупрочняемым относятся:
1) технический алюминий (сплав с содержанием примесей не более 1 %), обозначаемый буквой А с цифрой (например, А1);
2) алюминиево-марганцевый сплав (АМц);
3) алюминиево-магниевые сплавы (магналии) (АМг).
Вид обработки сплава обозначают буквами, добавленными через черточку к основной марке: М — отожженный (мягкий); Н — нагартованный; Н2 — полунагартованный; Т — закаленный и естественно состаренный; Т1 — закаленный и искусственно состаренный (при температуре 160… 180°С); Т4 — неполностью закаленный и искусственно состаренный; А — без обработки давлением; плак. — плакированный; Б — без плакирования.
Плакировкой называется покрытие листов из алюминиевых сплавов при прокатке тонким слоем (5 % от толщины листа с каждой стороны) чистого алюминия, предохраняющим основной металл от коррозии. Нагартовка и полунагартовка применяются для термически неупрочняемых сплавов, закалка и старение — для термически упрочняемых сплавов.
Особые группы сплавов составляют спеченные алюминиевые порошки (САП) и сплавы (САС), а также пенистый алюминий, получаемый при замешивании порошка гидрида титана в жидком алюминии. Пеноалюминий имеет плотность 300… 500 кг/м3, поэтому его можно применять как тепло — и звукоизоляционный материал.
Медь и ее сплавы. Медь в чистом виде имеет небольшую прочность и высокую пластичность. Температура ее плавления составляет 1 083 °С. Она плохо обрабатывается резанием, но хорошо деформируется в холодном и горячем состояниях. В строительстве медь применяется для водопроводных труб и кровельной черепицы.
Сплавы меди (латуни и бронзы) в строительстве применяются для декоративных целей (поручни, накладки, арматура для дверей и окон) и в сантехнике.
Латунь — сплав меди с цинком. Марки латуней обозначают буквой Л и цифрами, означающими содержание меди в процентах. Прочность латуней при растяжении Rp = 250…600 МПа. Для улучшения свойств латуни подвергают холодному и горячему деформированию, рекристаллизационному отжигу при температуре 500…700°С и легированию добавками Sn, Si, Mn, Al, Fe, Pb, повышающими прочность, коррозионную стойкость и антифрикционные свойства. Специальные латуни маркируют следующим образом: ЛА77-2 (латунь, содержащая 77 % Си, 2 % А1 и 21 % Zn); ЛАЖ60-1-1 (латунь, содержащая 60% Си, 1 % Al, 1 % Fe и 38 % Zn). Они представляют собой однородные твердые растворы и поэтому очень пластичны.
Оловянистая бронза представляет собой твердый раствор 4 — 5%-го олова в меди. При большем содержании олова пластичность и литейные свойства бронзы резко снижаются. Перед обработкой давлением бронзу подвергают рекристаллизационному отжигу при температуре 600…650°С. Для улучшения литейных свойств и повышения прочности в бронзу вводят до 1 % фосфора. Бронзы, обрабатываемые давлением, имеют прочность Rp — 350…400 МПа, пластичность 5 = 40…70% (после отжига) и 8 = 4… 12% (после холодной деформации).
Алюминиевые и кремнистые бронзы (сплавы меди с алюминием и кремнием) имеют механические свойства, аналогичные оловя — нистым бронзам, но более стойки в агрессивных средах.
Бериллиевые бронзы (сплавы меди с бериллием) содержат 2,0… 2,5 % Be и обладают наилучшими свойствами из всех бронз. После закалки при 760…780°С и старения при 300…350°С механические свойства бериллиевой бронзы составляют: Rv = 1 300… 1 350 МПа, 5 = 1,5%.
Свинцовые бронзы (сплавы меди со свинцом) содержат до 30 % свинца. Их компоненты не образуют твердых растворов. Они имеют невысокую прочность (Яр = 60 МПа) и пластичность (8 = 4 %).
Маркируют все бронзы аналогично латуням. Например: БрОЦСНЗ-7-5-1 — оловянистая бронза, содержащая 3 % Sn, 7 % Zn, 5% Pb, 1 % Ni и 84 % Си; БрАЖН 10-4-4 — алюминиевая бронза, содержащая 10% А1, 4% Fe, 4% Ni и 82% Си.
Титан и его сплавы. Титан — металл серебристо-белого цвета, плавящийся при температуре 1 665 °С. Существуют две модификации титана: при температуре ниже 882 °С — а-титан с гексагональной решеткой плотностью 4 505 кг/м3; при температуре 900 °С и выше — (3-титан с объемоцентрированной кубической решеткой плотностью 4 320 кг/м3. Технический титан марок ВТ1-00, ВТ1-0 и ВТ1-1 (Яр = 300…350 МПа, 8 = 20…30%) хорошо обрабатывается давлением и сваривается. Для улучшения свойств титан легируют добавками Al, Mo, V, Mn, Cr, Sn, Fe, Zn, Si.
Различают а-сплавы и (а + (З)-сплавы титана. Первые представляют собой твердые растворы с алюминием и легирующими элементами (Sn, Zn и Mo, Fe, Cr) в а-титане. Они не упрочняются термообработкой и подвергаются только рекристаллизационному отжигу при температуре 780… 850 °С. Вторые состоят из а и (3 твердых растворов и содержат кроме алюминия Cr, Mo, Fe. Они упрочняются закалкой и старением. Наиболее распространенные а-сплавы (ВТ5, ВТ5-1, ОТ4) имеют следующие показатели: Яр = = 700…950 МПа; 8 = 12…25%; (а + р)-сплавы (ВТ6, ВТ8, ВТ14) имеют следующие показатели: Яр = 950… 1 400 МПа; 8 = 8… 15 %. Титановые сплавы коррозионностойки, хорошо деформируются в горячем и холодном состояниях, поддаются сварке.
Изделия из цветных металлов. Цветные металлы дороже стали и чугуна, поэтому применяются в случаях, когда необходимы их специфические свойства: стойкость к коррозии, высокая теплопроводность, электропроводность, декоративные свойства, характерная для алюминия и его сплавов малая масса.
В качестве кровельных материалов применяются медь, алюминий и цинк-титановый сплав (П-цинк). Для устройства медной кровли по фальцевой технологии используют медную ленту, которая выпускается в рулонах. Алюминий применяется как для изготовления металлочерепицы, так и для устройства фальцевых кровель.
В европе достаточно распространены кровли из П-цинка — цинка, легированного титаном и медью.
Алюминиевые сплавы применяют для изготовления гнутых и прессованных профилей, штамповок, гофрированных листов различной формы. Из таких элементов выполняются различные сбор — но-разборочные и листовые конструкции, несущие конструкции навесных фасадов, трехслойные панели (типа «сандвич») наружных стен и покрытий, подвесные потолки, сайдинг, декоративные накладки, дверные и оконные переплеты.
Сплавы меди используют для производства водопроводных труб, фитингов, дверной и оконной фурнитуры, декоративных деталей интерьера и фасадов.
Изделия из стали, применяемые в строительстве
Строительные стали обозначают следующим образом: С235, С245, С255, С345, С590К…, где буква С означает, что сталь стро-
|
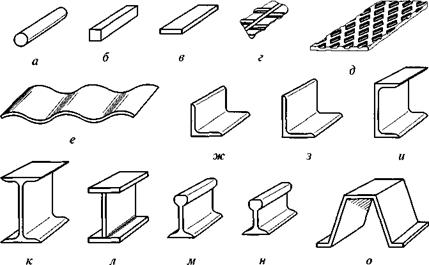
Рис. 6.7. Стальной прокат: а — круглый; б — квадратный; в — полосовой; г — периодического профиля; д — листовой рифленый; е — листовой волнистый; ж — уголок равнобокий; з — уголок неравнобокий; и — швеллер; к — двутавр; л — двутавр сварной; м — рельс крановый; н — рельс железнодорожный; о — шпунтовая свая |
|
|
|
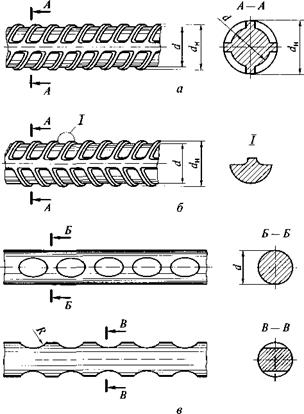
г Рис. 6.8. Стальная арматура: а — класса А-П; 6 — класса А-III; в — проволока периодического профиля; г — семипроволочная арматурная прядь |
ительная; цифры означают предел текучести, МПа, а буква К — вариант химического состава. Буква Д в конце марки стали означает, что сталь дополнительно легирована 0,15…0,30 % меди (например: С345Д).
Для стальных конструкций используются в основном изделия из стального проката, а также из гнутых и сварных профилей. Прокатка стали заключается в том, что раскаленные стальные заготовки многократно пропускают между вращающимися навстречу
|
Таблица 6.1
|
друг другу валками прокатного стана. Проходя в зазоре между валками, горячий металл пластически деформируется, сжимаясь в поперечном сечении и вытягиваясь в длину, в результате чего он превращается в длинномерное изделие с постоянным поперечным сечением определенной формы.
Стальной прокат подразделяется на несколько видов (рис. 6.7). Сортовой прокат включает в себя полосы, прутки круглого, квадратного и шестигранного сечений. Фасонный прокат имеет сложный профиль поперечного сечения: уголок (равнобокий и неравнобокий), швеллер, тавр, двутавр. Листовой прокат включает в себя листовую сталь, сталь универсального или специального назначения, гладкую или рифленую сталь, а также кровельное железо, листовое, рулонное, профилированное (волнистое или трапециевидное) железо, металлочерепицу. Специальный прокат включает в себя шпунт, сваи, арматуру, трубы, рельсы и др. Основным видом специального проката для строительства является стальная арматура для бетона (рис. 6.8).
Арматура подразделяется на классы: А — стержневая арматура; В — проволока; К — арматурные канаты. Основные нормируемые характеристики стержневой арматуры приведены в табл. 6.1.
Символы в обозначении класса арматуры означают следующее: А — стержневая; т — термически обработанная; с — для районов Севера; С — свариваемая; К — коррозионностойкая.
Арматура класса A-І — гладкая; остальных классов — периодического профиля. Арматурную проволоку выпускают диаметром от 3 до 8 мм и подразделяют по форме поперечного сечения на гладкую (В) и периодического профиля (Вр).
Ассортимент изделий из стального проката и гнутых профилей очень широк. В строительстве используются стальные двери, ворота, заборы, ограждения, решетки, лестницы, перила, поручни, строительные леса, водосточные и вентиляционные трубы, короба, козырьки, арматурные сетки и каркасы, сетки и столбы для заборов и ограждений. Соединения деталей и элементов строительных конструкций выполняются с помощью крепежных изделий, как правило, стальных. Это — заклепки, болты, винты, шурупы, гвозди, анкера, кронштейны. Для соединения железобетонных элементов служат заанкеренные в бетон стальные закладные детали, наружные части которых свариваются между собой.
Химико-термическая обработка стали
При химико-термической обработке происходит изменение не только структуры, но и химического состава сплава.
Химико-термическая обработка заключается в насыщении поверхностных слоев стали различными элементами: углеродом (цементация), азотом (азотирование), углеродом и азотом одновременно (цианирование), бором (борирование) и др. При этом свойства поверхностного слоя становятся отличными от свойств сердцевины детали, что позволяет сочетать несовместимые обычно высокие значения твердости и ударной вязкости. Высокую твердость придают поверхностному слою, что обеспечивает износостойкость деталей, а сердцевинную часть делают ударопрочной, способной воспринимать динамические нагрузки.
Цементации подвергают низкоуглеродистые стали, содержащие 0,1… 0,2 % углерода. Их насыщают углеродом до его концентрации в поверхностном слое 0,8… 1,0 % С и затем подвергают закалке, в результате которой цементованный слой толщиной 0,5…2,5 мм приобретает структуру мартенсита и высокую твердость. Сердце — вина изделия, содержащая слишком мало углерода, не закаливается и остается ударно-вязкой и пластичной.
Науглероживание производят в твердой или газовой среде, называемой карбюризатором.
При твердой цементации детали укладывают в стальные ящики, пересыпая их карбюризатором — древесным углем или коксом (слоем толщиной 3… 10 мм) с активизаторами BaC03, Na2C03 в количестве 10…40%. Ящики закрывают крышками, герметизируют огнеупорной глиной и ставят в печь. При температуре 930…950°С — выше линии GS (см. рис. 6.6) — образующиеся активные атомы углерода диффундируют в решетку у-железа.
При газовой цементации стальные детали нагревают в газовых смесях, содержащих метан, пропан, бутан и др.
Азотирование — процесс насыщения поверхностного слоя стали азотом. Процесс азотирования заключается в выдержке деталей в течение длительного времени (до 60 ч) в атмосфере аммиака при температуре 500…600°С. Аммиак при нагреве разлагается на азот и водород. Активные атомы азота проникают в решетку а — железа, образуя нитриды железа. Высокую твердость азотированному слою придают нитриды легирующих элементов: хрома, молибдена, алюминия. Поэтому азотированию обычно подвергают легированные стали.
По сравнению с цементацией азотирование стали дает более высокие твердость и износостойкость поверхностного слоя, высокие коррозионные свойства и усталостную прочность. После азотирования не требуется закалки, что позволяет избежать сопутствующих ей дефектов.
Цианирование — процесс совместного насыщения поверхности стали азотом и углеродом. При цианировании нагрев изделий осуществляется либо в расплавленных солях, содержащих цианистый натрий (NaCN), либо в газовой смеси метана (СН4) и аммиака (NH3).
При низкотемпературном цианировании (500…600°С) поверхностный слой насыщается преимущественно азотом на глубину 0,01 …0,04 мм. После низкотемпературного цианирования отпуск не проводят.
Высокотемпературное цианирование (850… 950 °С) применяют для получения глубины обработанного слоя 0,6… 1,8 мм. Процесс занимает от 3 до 10 ч, после чего детали подвергают закалке и низкому отпуску. По сравнению с цементованным цианированный слой имеет более высокие твердость и износостойкость, а также более высокое сопротивление коррозии. Недостатком цианирования является высокая стоимость процесса, связанная с применением мер безопасности в связи с высокой токсичностью цианистых солей.
Борирование придает поверхностному слою очень высокие твердость, износостойкость и устойчивость к коррозии в различных средах. Насыщение бором часто проводят при электролизе расплавленной буры (Na2B407); при этом стальная деталь служит катодом. Борирование также производят в расплавленных солях или газовых средах, содержащих соединения бора. Диффузионный слой состоит из боридов железа и имеет толщину 0,1 …0,2 мм.
Термомеханическая обработка (ТМО) металлов заключается в сочетании пластической деформации стали в состоянии аустенита с закалкой. Наиболее распространен высокотемпературный способ, при котором сталь деформируют на 20… 30 % при температуре устойчивого аустенита, после чего следуют немедленная закалка и низкотемпературный отпуск. Такая комбинированная обработка позволяет получать очень высокую прочность стали при хорошей пластичности и вязкости.
Термическая обработка стали
Термическая обработка стали основана на зависимости структуры от скорости охлаждения аустенита. При термической обработке изменяется только структура стали; химический состав остается неизменным. Нагрев стали с переходом температуры через критическую точку 727 °С вызывает превращение перлита в аустенит. При медленном охлаждении аустенит переходит в перлит, а при резком — в мартенсит. При этом атомы железа, так же как и при медленном охлаждении, перестраиваются из решетки у-же — леза в решетку a-железа, но атомы углерода не успевают покинуть у-решетку и оказываются зажатыми в решетке a-железа, где в нормальных условиях углерода не может содержаться более 0,01 %.
Таким образом, получается сильно пересыщенный твердый раствор углерода в a-железе, называемый мартенситом.
Углерод искажает решетку a-железа, сообщая ей высокие внутренние напряжения, обусловливающие высокую твердость и хрупкость стали. Эти напряжения вызывают стремление углерода к выходу из решетки a-железа путем диффузии, образованию цементита и тем самым распаду мартенсита на феррит и цементит. Этот процесс при нормальных температурах заторможен, но при нагревании он может пойти достаточно быстро с превращением мартенсита в перлит.
При невысоком нагреве мартенсита могут получаться промежуточные структуры, которые отличаются от перлита гораздо меньшим размером кристаллов феррита и цементита: троостит (коллоидный раствор цементита в феррите) и сорбит (тонкодисперсная смесь феррита и цементита). Эти структуры имеют меньшую, чем у мартенсита, но достаточно высокую твердость и в то же время обладают значительной ударной вязкостью.
Закалка стали. Закалка стали проводится с целью повышения ее твердости. При закалке доэвтектоидную сталь нагревают до температуры на 30… 50 °С выше линии GS(см. рис. 6.6), а заэвтектоид — ную — на 30… 50 °С выше линии SK. Заэвтектоидная сталь не требует нагрева до полного превращения в аустенит, так как не имеет смысла заменять цементит другой структурой, потому что ничего тверже цементита получить нельзя. После определенной выдержки нагретые изделия резко охлаждают, погружая их в воду, масло, растворы или расплавы солей. Мартенсит получается при самой высокой скорости охлаждения (в воде), троостит — при меньшей скорости (в масле), сорбит — при еще более медленном, охлаждении (в расплавах солей).
В результате закалки значительно возрастают твердость, износостойкость, а также прочность стали, но резко снижаются ее пластичность и ударная вязкость.
Отпуск стали. Отпуск стали проводится с целью уменьшения хрупкости закаленной стали путем устранения внутренних напряжений, возникающих при закалке. Закаленную сталь нагревают до температуры, не превышающей 727 °С, и выдерживают определенное время. Чем выше температура отпуска, тем полнее снимаются напряжения. При отпуске стали происходит переход мартенсита в более устойчивые структуры за счет диффузии углерода при повышении температуры. Фазовых превращений при этом не происходит. Различают следующие виды отпуска:
• низкий отпуск (150…200°С) — повышается прочность и незначительно ударная вязкость, твердость почти не снижается. Структура после отпуска — мартенсит;
• средний отпуск (350…500°С) — повышается пластичность, немного снижается твердость. Структура после отпуска — троостит;
• высокий отпуск (500…680 °С) — возрастает ударная вязкость, снижается твердость. Структура после отпуска — сорбит.
Отжиг стали. Отжиг стали отличается от закалки очень медленным охлаждением изделий вместе с печью или под слоем песка, золы, шлака.
Отжиг I рода проводят с целью устранения физической или химической неоднородности стали, независимо от того, протекают при этом фазовые превращения или нет. Различают:
• диффузионный отжиг (1 100… 1 200°С) — для выравнивания химического состава стали по объему за счет диффузии углерода в аустените;
• рекристаллизационный отжиг (680…730°С) — для выравнивания неоднородностей кристаллического строения, образовавшихся в результате деформаций стали в холодном состоянии (устранение наклепа);
• отжиг для снятия остаточных напряжений (160…700°С), которые возникают при сварке, механической обработке, ковке и т. д.
Отжиг Ирода проводят с целью повышения пластичности и снижения твердости стали (для лучшей обрабатываемости). Это достигается путем замены метастабильных структур (мартенсита, троости — та, сорбита) равновесными (ферритом, перлитом, цементитом).
При отжиге II рода сталь нагревают до тех же температур, что и при закалке, выдерживают до полного завершения фазовых переходов (получения структуры аустенита) и медленно охлаждают, чтобы обеспечить распад аустенита и избежать образования сорбита. Скорость охлаждения для углеродистых сталей обычно составляет 100… 150°С/ч, для легированных сталей — 40…60°С/ч.
Структура и фазовый состав железоуглеродистых сплавов
Структура и фазовый состав сплавов изучаются с помощью диаграмм состояния, изображаемых в координатных осях «состав — температура». Построение диаграмм состояния описано в подразд.
9.8. Для двухкомпонентных сплавов ось составов изображается в виде отрезка, по концам которого указывают символы компонентов (условно А и В) (рис. 6.3). От точки В к точке А содержание компонента А в сплаве возрастает от 0 до 100%, а содержание компонента В уменьшается до 0 от 100 %. В любой точке оси сумма концентраций компонентов А и В равна 100 %. Состав, характеризуемый точкой / на оси АВ, можно определить по правилу отрезков, согласно которому содержание компонентов в процентах равно умноженному на 100 отношению длин соответствующих отрезков к длине оси: А = (ІВ/АВ) 100; В = (АІ/АВ) 100.
|
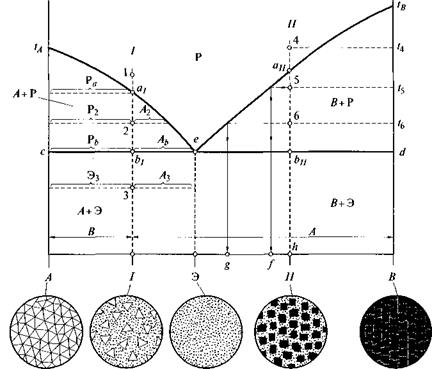
Рис. 6.3. Диаграмма состояния сплава, компоненты которого образуют в твердом состоянии механические смеси своих кристаллов |
Диаграмма состояния, изображенная на рис. 6.3, характеризует сплав, компоненты которого в жидком состоянии неограниченно растворимы друг в друге, а в твердом состоянии образуют механические смеси (не образуют твердых растворов и химических соединений).
Точки 1А и tB — температуры кристаллизации свободных компонентов А и В (буквами Aw В обозначаются также кристаллы этих компонентов в составе структуры сплава); Э — эвтектика — особая структура, представляющая собой механическую смесь одновременно кристаллизовавшихся из жидкости и поэтому очень мелких и тесно перемешанных кристаллов компонентов А и В, содержание которых пропорционально соответственно отрезкам ЭВ и АЭ] е — эвтектическая точка, указывающая на состав эвтектики и температуру ее кристаллизации, начало и конец которой, в отличие от других составов, совпадают.
Эвтектика — не фаза, а структурная составляющая (элемент структуры сплава), поэтому ее 100%-е содержание в отличие от компонентов отмечается на диаграмме штриховой линией.
Кривая tAetB — кривая температур начала кристаллизации сплава, или кривая верхних критических точек, называемая ликвидусом (от лат. liquidus — жидкий). Выше ликвидуса сплав находится в расплавленном состоянии (Р — расплав). Линия ced — линия температур конца кристаллизации сплава, или линия нижних критических точек, называемая солидусом (от лат. solidus — твердый). Ниже солидуса сплав состоит из твердых кристаллов (А, В и Э). Между ликвидусом и солидусом существуют жидкая (Р) и твердые (А и В) фазы одновременно.
Температуры начала и конца кристаллизации сплава / соответствуют точкам а, и bh сплава II — точкам аи и Ь„.
Проведем через точку 2 горизонтальную линию до границ области tAec. Эта линия является осью фазовых составов, по концам которой имеем: слева — 100 % компонента А, а справа (на границе с расплавом) — 100 % расплава. Это отмечено буквами А + Р. В данной области из расплава при охлаждении выделяются кристаллы компонента А. В области etBd записано В + Р, так как здесь из расплава выделяется в твердом состоянии компонент В. Точка 2 делит ось фазовых составов А — Р на отрезки Аг и Р2, измерив которые, можно определить процентные содержания фаз А и Р в сплаве I при температуре в точке 2.
Характер изменения фазового состава сплава / при понижении температуры можно проследить, строя оси фазовых составов для различных точек на вертикали /. Сравнение отрезков в точках ah 2 и Ь/ показывает, что при понижении температуры от точки а/ до точки bj содержание компонента А увеличивается от 0 (Аа = 0) до [Ab/(Ab + Pfc)]100 = 44%, а содержание расплава уменьшается от 100 % до [РЬ/(АЬ + РА)]100 = 56 %. В точках Ь, и 3 имеем: РА = Э3 и Аь — А3, т. е. то количество компонента А, которое выделилось из расплава, пока он оставался жидким, существует теперь в твердом сплаве, а расплав, который в конце кристаллизации (в точке Ь[) составляет около 56 % сплава, превращается в эвтектику. Соответственно в областях АсеЭ и 3edB указано А + Э и В + Э.
Проследим за изменением состава расплава в сплаве II при охлаждении. При температуре t4 (точка 4) и ниже, вплоть до точки О//, сплав полностью жидкий, поэтому состав расплава и состав сплава — одно и то же (точка h на оси составов). В точке ап начинается кристаллизация расплава и из него выделяются первые кристаллы компонента В. В результате частичной потери этого компонента изменяется состав и количество расплава. Для определения состава расплава при температуре /5 из точки 5 проведем горизонтальную прямую линию до границы с расплавом и опустим перпендикуляр на ось составов в точку / При более низкой температуре 16 состав расплава будет характеризоваться точкой g, а в конце кристаллизации (в точке Ьц) он будет соответствовать составу эвтектики. Следовательно, при охлаждении сплава II содержание компонентов А и В в жидкой фазе (состав расплава) изменяется по кривой а, р. Аналогично по кривой ар изменяется состав расплава при кристаллизации сплава /.
Рассмотрим, как формируются структуры сплава в зависимости от его состава. Изобразим условно кристаллы компонента А треугольниками, а компонента В — квадратиками; тогда структура эвтектики будет представлена смесью треугольников и квадратиков, только очень мелких, практически не различимых на фоне крупных кристаллов чистых компонентов. Площади, занимаемые в эвтектике треугольниками (компонентом А) и квадратиками (компонентом В) составляют соответственно 57,5 и 42,5 %, что соответствует отрезкам ЭВ и АЭ оси составов. Для того чтобы определить структуру сплава /, измерим длины отрезков Э3 и А3 и по ним вычислим процентное содержание в сплаве компонента А и эвтектики. Получим 44 и 56%. Следовательно, площадь, занятая крупными треугольниками на картинке структуры сплава /, должна составлять 44 % от общей площади, а оставшаяся площадь должна приходиться на долю эвтектики, изображаемой точками. Аналогичным образом, измерив отрезки Э/z и hB (с учетом того, что крупные кристаллы в данном случае — квадратики), получим структуру сплава //.
Для решения обратной задачи — определения состава сплава по его структуре — нужно измерить площади, занимаемые элементами структуры, и с помощью диаграммы определить состав сплава.
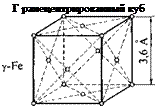
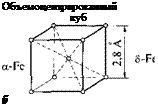
Структура чистого железа. Чистое железо при охлаждении или нагревании претерпевает ряд превращений в твердом состоянии, которые дают критические точки на кривой охлаждения (рис. 6.4). В интервалах между этими точками железо существует в виде четырех модификаций (а-, (}-, у- и 5-Fe), из которых y-Fe имеет гранецентрированную кубическую (ГЦК) кристаллическую решетку с параметром 3,6 А, а остальные — объемоцентрированную кубическую (ОЦК) с параметром 2,8 А. Часто p-Fe и 8-Fe отдельно не выделяют и рассматривают как a-модификацию. Переход у —> ос (911 °С) при охлаждении или а у при нагревании играет главную роль в формировании свойств стали.
Фазы в структуре стали. Углерод и железо в зависимости от температуры образуют жидкий раствор (расплав Р), два твердых раствора — феррит (Ф) и аустенит (А) — и химическое соединение Fe3C, называемое цементитом (Ц).
Феррит — твердый раствор углерода в a-железе, существующий при температурах ниже 911 °С. Растворимость углерода в а — железе мала (не более 0,02 %), так как в плотной решетке а-желе — за углерод может находиться, только замещая атомы железа, что требует высокой энергии.
Аустенит — твердый раствор углерода в у-железе, существующий при температурах выше 727 °С. Ниже 727 “С аустенит распада-
1539 °С (Точка застывания)
 5-Fe 1392 “с (Перестроение решетки)
5-Fe 1392 “с (Перестроение решетки)
Охлаждение
y-Fe
911 °С (Перестроение Ре х решетки)
(парамагнитно)
‘ 770 °С
(Изменение о-Fе магнитных
(ферромагнитно) свойств
Время
а
Рис. 6.4. Кривая охлаждения чистого железа (а) и структура кристалли-
ческой решетки модификаций железа {б)
ется на феррит и цементит. В у-железе углерод растворяется до 2,14%. В этом случае углерод внедряется между атомами железа благодаря тому, что у-решетка не так плотно упакована.
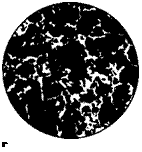
Структура углеродистой стали. Структура углеродистой стали при нормальной температуре образована двумя фазами (двумя типами кристаллов): очень мягким и пластичным ферритом и очень твердым и хрупким цементитом. Чем больше в стали углерода, тем больше образуется цементита и меньше феррита и тем выше твердость и ниже пластичность стали. При содержании углерода менее 0,01 % сталь состоит из одного только феррита (рис. 6.5, а).
Если сталь содержит 0,8 % углерода, то ее структура представляет собой эвтектоидную (похожую на эвтектику) смесь мелких кристаллов феррита (88%) и цементита (12%), называемую перлитом (П). При 200-кратном увеличении кристаллы феррита и цементита в перлите практически неразличимы, в то время как кристаллы феррита, выделившиеся ранее из аустенита, являются достаточно крупными (см. рис. 6.5, б). Структура перлита видна только при большом увеличении (рис. 6.5, в). При содержании углерода менее 0,8 % структура стали включает в себя перлит и феррит, при содержании углерода более 0,8 % — перлит и цементит (рис. 6.5, г).
 |
Рис. 6.5. Структура сталей с содержанием
углерода:
а — 0 % (феррит); б — 0,4 % (феррит + перлит);
в — 0,8% (перлит); г — 1,2% (цементит + пер-
лит) (а, б, г — увеличение в 200 раз; в — увеличе-
ние в 800 раз)
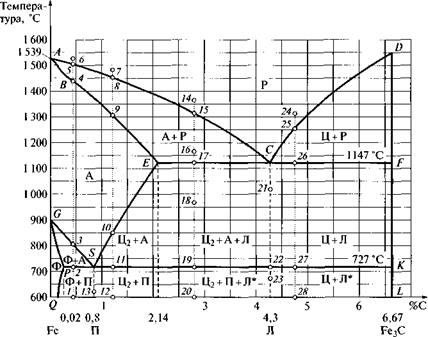
Диаграмма состояния железоуглеродистых сплавов. Диаграмма состояния Fe — Fe3C (рис. 6.6) является только частью полной диаграммы Fe — С, поэтому углерод как фаза на диаграмме отсутствует. В этой части диаграммы цементит, являющийся одной из фаз, играет роль второго компонента, хотя им и не является (второй компонент — углерод). Первый компонент — железо — также не фигурирует на диаграмме, поскольку всегда растворяет в себе некоторое количество углерода и представляет собой твердый раствор (феррит или аустенит).
Кривая ACD — ликвидус. Выше ликвидуса находится область расплава (Р). Кривая BECF— солидус. Ниже солидуса все сплавы — твердые. В области BESG — это твердый раствор аустенит, а в области ECFKS — механические смеси аустенита и цементита с эвтектикой, которая называется ледебуритом (Л). Сплав (чугун) с содержанием углерода 4,3 % полностью состоит из эвтектики. Он имеет самую низкую температуру плавления (кристаллизации) — 1 147 °С (точка С). При t > 727 °С ледебурит представляет собой механическую смесь мелких кристаллов аустенита и цементита, а при t < 727 °С — перлита и цементита.
Дело в том, что твердый раствор (аустенит) разлагается при охлаждении аналогично жидкому раствору (расплаву) с выделением тех или иных растворенных веществ. Поэтому пересечения линий диаграммы в точках S и С сходны между собой. Точка S
называется эвтектоидной точкой, т. е. похожей на эвтектическую точку С. Структура, образующаяся в точке S — это перлит. Кривая GSE — это кривая температур начала разложения аустенита. На участке GS (в области GSP) из аустенита выделяется феррит, а на участке SE (в области SEFK) — цементит (вторичный). Линия PSK — линия температур конца разложения аустенита, или линия эвтектоидных превращений. Ниже этой линии аустенит не существует. Он превращается в перлит.
 |
Рассмотрим процессы при нагревании доэвтектоидной стали, содержащей 0,4 % углерода (точка /). Пока температура не достигнет 727 °С (линия PS), сталь будет состоять из феррита и перлита (Ф + П). При температуре 727 °С (точка 2) перлит (П) превращается в аустенит (А), так как a-железо переходит в у-железо. В феррите же (Ф) сохраняется a-модификация железа и он остается в стали. При повышении температуры более 727 °С количество феррита уменьшается, он растворяется в аустените. В точке 3 содержание феррита будет 0 %, а содержание аустенита — 100 %.
|
Доэвтек- тоидная |
Заэвтек- тоидная |
Доэвтектический |
Заэвтектический |
|
( |
Зталь |
Ч |
/гул |
|
Рис. 6.6. Диаграмма состояния Fe — Fe3C |
Сталь в отличие от чугуна при нагревании полностью переходит в фазу аустенита. Дальнейший нагрев приводит к плавлению стали. Первые капли расплава появятся при температуре в точке 4. Затем количество расплава будет увеличиваться, а количество аустенита — уменьшаться, пока он полностью не растворится в расплаве (в точке 5).
При охлаждении сплава все будет происходить в обратном порядке. При очень медленном (равновесном) охлаждении образуется первоначальная структура стали, состоящая из феррита и перлита. Такую структуру называют равновесной. При быстром охлаждении возникают неравновесные (метастабильные) структуры, характеризующиеся высокой твердостью. На этом основана закалка стали.
Рассмотрим процессы, происходящие при охлаждении заэв — тектоидной стали с содержанием углерода 1,2%. При температуре в точке 8 начинается кристаллизация расплава; из него выделяются кристаллы аустенита. С понижением температуры твердой фазы (аустенита) становится все больше, а жидкой — все меньше. В точке 9 заканчивается переход расплава в аустенит. В виде аустенита сплав существует до точки 10. Начиная с этой температуры аустенит разлагается — из него выделяется цементит. Этот цементит называют вторичным (Ц2), чтобы отличать его от цементита (Ц), выделяющегося в области CDF из расплава и не имеющего ограничений в росте и расположении кристаллов. Вторичный цементит выделяется в крайне стесненных условиях, поэтому его кристаллы являются очень мелкими и располагаются в виде узких прослоек по границам кристаллов аустенита (см. рис. 6.5, г). Выделение вторичного цементита заканчивается в точке 11. Количество выделившегося вторичного цементита в нашем сплаве составляет 6,8 %. Оставшийся к концу разложения аустенит (93,2 %) при температуре 727 °С переходит в перлит, т. е. распадается на смесь мелких кристаллов феррита и цементита.
Свойства углеродистой стали. Методы испытаний
Углеродистая сталь имеет следующие значения свойств: плотность — 7 850 кг/м3; предел прочности при растяжении — 300…700 МПа; относительное остаточное удлинение после разрыва — 12…40%; модуль упругости — 2,1 • 105 МПа; коэффициент внутренней теплопроводности — 50…70 Вт/(м ■ К).
Влияние углерода. С увеличением содержания углерода возрастает твердость стали, а ее пластичность и ударная вязкость снижаются. Прочность с повышением содержания углерода сначала растет до максимального значения (при содержании углерода в стали 0,8… 1,0 %), а затем снижается. С увеличением содержания углерода ухудшаются свариваемость, а также способность стали деформироваться в горячем и особенно в холодном состояниях.
Влияние примесей. Марганец и кремний полезны — они повышают прочность стали. Сера снижает пластичность и вязкость стали, а также придает стали красноломкость (хрупкость при горячем деформировании). Фосфор в количестве до 1,2 % увеличивает прочность, но снижает пластичность, а также способствует охрупчиванию стали, повышая температурный порог хладноломкости.
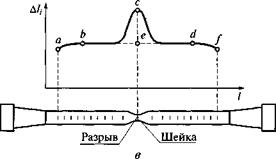
Прочность и пластичность стали. Прочность и пластичность стали определяют испытанием на растяжение образцов цилиндрической формы, получаемых токарной обработкой, или плоских образцов, вырезаемых из листового проката (рис. 6.1). Головки образцов при испытании вставляют в захваты разрывной машины. Используют также натуральные образцы — стержни определенной длины, отрезаемые от сравнительно тонких длинномерных профилей (например, образцы арматуры для бетона). Они не имеют головок и требуют применения зажимающих захватов.
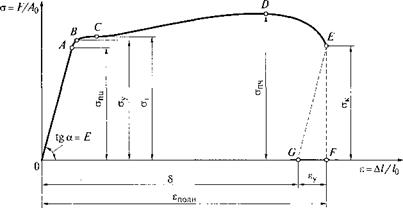
Зависимость растягивающих напряжений от относительного удлинения образца для мягкой стали имеет вид, показанный на рис. 6.2. На кривой растяжения имеются характерные точки (А, В, С, D), которым соответствуют четыре прочностные характеристики: предел пропорциональности (опц), предел упругости (ау), предел текучести (о.,) и предел прочности (апч). Диаграмма растяжения дает также характеристику пластичности стали — относительное остаточное удлинение после разрыва: 5 = (/к — /0)//0, где /к — длина расчетной части после разрыва; /0 — расчетная длина до испытания.
Величина 6 — единственная из всех характеристик, зависящая от расчетной длины, что обусловлено неравномерным удлинени — ( П I I И II I П I И I ( 1 П I п ( TQ
1
|
Рис. 6.1. Образцы для испытания на растяжение (а — цилиндрический; 6 — плоский) и график распределения удлинения отдельных участков по длине образца (в) |
|
Рис. 6.2. Диаграмма растяжения отожженной (мягкой) стали: ок — конечное значение напряжения |
ем образца (рис. 6.1, в). Для определения 6 по длине образца наносят риски, например через каждые 5 мм. После испытания каждое деление увеличит свою длину на А/,. При нагружении образца до точки D на диаграмме растяжения (см. рис. 6.2) все деления получают в основном одинаковые остаточные удлинения А/, и график их распределения представляет собой горизонтальную прямую линию bed (см. рис. 6.1, в). Снижение А/, по концам рабочей части образца (участки ab и df) является результатом влияния головок. При дальнейшем растяжении промежутки, близкие к разрыву, получают дополнительное удлинение за счет образования местного сужения (шейки) и общее распределение А/, характеризуется кривой abcdf.
Уменьшение площади поперечного сечения в шейке приводит к падению нагрузки при испытании (участок DE), но не к падению фактических напряжений (см. рис. 6.2). Расчетные же напряжения, показанные на диаграмме растяжения (см. рис. 6.2), прямо пропорциональны нагрузке, так как образование шейки при их расчете не учитывается.
Для сравнимости результатов определения 5 на образцах разных размеров и формы расчетная длина /0 (длина, на которой
определяется 5) должна выбираться равной 11,3л/Д, или 5,65 где Ап — площадь поперечного сечения образца до испытания. Тогда для круглых образцов /0 = 10г/0 или /0 = 5d0, где d0 — первоначальный диаметр. Значение 5 десятикратных образцов всегда будет меньше, чем пятикратных (8Ш < б5).
На значение 5 влияет также положение разрыва по длине. Максимальное значение, получаемое при разрыве посередине /0, принято в качестве нормы при определении 5.
Таким образом, при определении 8 измеряют d0 (или А0) образца, рассчитывают /0 и определяют число промежутков п на расчетной длине (Я|0 и п5). После испытания половинки образца складывают и отсчитывают половину промежутков (п/2) вправо от разрыва и половину — влево от разрыва. Измеряют расстояние между полученными крайними рисками, что дает значение конечной длины /к для расчета 8.
Наряду с 8 используется и другая характеристика пластичности стали — относительное остаточное сужение после разрыва у/ = = (А0 — Аш)/А„, где Аш — площадь шейки.
Твердость стали. Твердость стали определяют чаще всего методом Бринелля — вдавливанием шарика (см. подразд. 2.5). Сравнимость результатов при различном диаметре шарика обеспечивается постоянством отношения нагрузки Р к квадрату диаметра D шарика: Р/D2 = const. Твердость по Бринеллю НВ = Р/Асф, где F — нагрузка; Асф — площадь сферической поверхности отпечатка. Метод Бринелля применяют для сталей с твердостью не более 450 кгс/мм2 (4,5 ГПа).
Ударная вязкость стали. Ударную вязкость стали определяют на маятниковом копре (см. подразд. 2.5). Стальной образец имеет форму балочки квадратного сечения 10×10 мм и длину 55 мм. По методу Шарпи образец лежит на опорах свободно и имеет надрез глубиной 2 мм на стороне, противоположной удару маятника (см. рис. 2.7). Надрез позволяет сосредоточить энергию удара в одном месте. Ударная вязкость характеризуется отношением работы U, затраченной на разрушение образца, к площади поперечного сечения А: и= U/ А. Единица измерения ударной вязкости — Дж/м2.
Углеродистые и легированные стали
Углеродистые стали в зависимости от содержания вредных примесей (серы и фосфора) подразделяются на следующие группы.
1. Сталь углеродистая обыкновенного качества (ГОСТ 380 — 94) предназначена для изготовления проката, труб, ленты, проволоки и других изделий. Она содержит углерода от 0,06 до 0,49 %. Эту сталь получают в мартеновских печах и кислородных конверторах. В зависимости от содержания углерода, марганца и кремния сталь подразделяется на следующие марки: СтО, Ст1, Ст2, СтЗ, Ст4, Ст5, Стб. В конце обозначения указывают способ раскисления: «кп» — кипящая, «пс» — полуспокойная, «сп» — спокойная (например: СтЗкп). Чем выше марка стали, тем больше в ней содержится углерода. Содержание вредных примесей не должно превышать: серы — 0,05%; фосфора — 0,04% (кроме марки СтО, для которой допускается серы до 0,06 % и фосфора до 0,07 %).
2. Углеродистые стали повышенного качества (ГОСТ 1050 — 88) выплавляются в электропечах, конвертерах, мартеновских печах. К ним предъявляются более жесткие требования по содержанию вредных примесей (S < 0,04 %, Р < 0,035 %). Эти стали маркируют двузначными цифрами 05, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, указывающими среднее содержание углерода (в сотых долях процента).
3. Высококачественные углеродистые и легированные стали (S < 0,025 %, Р < 0,025 %) в конце марки обозначаются буквой А (например: У10А). Буква У означает углеродистую сталь, а цифра — содержание углерода (в сотых долях процента). Легированные стали получают добавлением специальных присадок (легирующих элементов) с целью улучшения механических и физико-химических (электропроводности, жаростойкости, коррозионной стойкости и др.) свойств. По содержанию легирующих элементов различают стали низколегированные (до 2,5%), среднелегированные (2,5… 10,0%) и высоколегированные (более 10%).
В качестве главных легирующих элементов применяют хром (до 2%), никель (1…4%), марганец (до 2%), кремний (0,6… 1,2%). Часто сталь легируют не одним, а несколькими элементами. Например: Сг и Ni (хромоникелевая сталь), Сг и Мп (хромомарганцевая сталь), Сг, Ni, Mo, V (хромоникельмолибденованадиевая сталь). Такие легирующие элементы, как Mo, W, V, Ті, обычно вводят в сталь в сочетании с Сг, Ni.
В обозначении марок конструкционных сталей первые две цифры означают содержание углерода (в сотых долях процента). Затем следуют буквы, обозначающие легирующие элементы (X — хром, Н — никель, В — вольфрам, М — молибден, Ф — ванадий, Т — титан, Ю — алюминий, Д — медь, Г — марганец, С — кремний, К — кобальт, Ц — цирконий, Р — бор, А — азот, Б — ниобий). Цифра после буквы означает среднее содержание данного элемента (в целых процентах). Отсутствие цифры означает, что содержание данного элемента — около 1 % или меньше. Например, сталь 18ХГТ содержит около 0,18 % С и не более, чем по 1 % Сг, Мп и Ті; сталь 38ХНЗМФА содержит в среднем 0,38…0,40% С, около 3 % Ni и не более, чем по 1 % Сг, Mo, V. Буква А в конце марки означает, что сталь высококачественная.
Сущность процессов получения чугуна и стали
Получение чугуна. Получение чугуна в доменной печи заключается в восстановлении железа из оксидов железной руды, в качестве которой используют магнитный железняк (минерал магнетит — Fe304); красный железняк (гематит — Fe203); бурый железняк (минералы лимонит — 2Fe203- ЗН20 и гетит — Fe203- Н20) и др.
Чтобы отделить примеси, содержащиеся в руде и коксе (продукте переработки каменного угля), их нужно расплавить, однако температура плавления у них намного выше, чем у чугуна. Ее понижают, вводя флюсы (плавни), чаще всего — известняк.
Загружаемая сверху в доменную печь шихта, содержащая железную руду, кокс и флюсы, постепенно перемещается вниз и попадает в зоны все более высокого нагрева. В нижней части домны (горне) температура возрастает до 1 600 °С. Сюда стекают жидкие чугун и шлак. Более легкий шлак скапливается над чугуном. Периодически шлак и чугун выпускают и направляют для дальнейшей переработки.
Вдуваемый в доменную печь воздух, нагретый до 700…800°С, обеспечивает горение кокса с образованием окиси углерода (СО), которая отнимает кислород у оксидов железа:
3Fe203 + СО = С02 + 2Fe304 -> Fe304 + СО = С02 + 3FeO -»
-> FeO + СО = С02 + Fe
При температуре около 1 000 °С имеет место науглероживание восстановленного железа и превращение его в чугун:
2СО + 3Fe = С02 + Fe3C
Пустая порода и флюсы также претерпевают определенные превращения и переходят в шлак. Азот воздуха, СО и С02 образуют доменный газ, удаляемый из домны через колошник по газопроводам.
В материалах шихты имеются вещества, дающие чугуну полезные (марганец, кремний) и вредные (сера, фосфор) примеси. Сера может быть удалена из чугуна при сильнооснбвном шлаке и высокой температуре процесса. Фосфор же удалить из чугуна нельзя. Чтобы чугун не содержал фосфора, шихта должна быть свободна от Р205.
Получение стали. Получение стали заключается в удалении из чугуна углерода путем его окисления (выгорания). Попутно выгорают и примеси: кремний, марганец, фосфор. Сера удаляется с трудом, поэтому для получения стали используется бессернистый чугун. В отличие от доменного процесса переработка чугуна в сталь происходит при более высокой температуре, так как сталь более тугоплавка, чем чугун. Повышение температуры достигается за счет теплоты, выделяющейся в основном при выгорании примесей. Горение углерода дает слишком мало теплоты и не может обеспечить повышение температуры. Теплота может дополнительно подводиться извне.
Сталь получают в конверторах, мартеновских печах и электропечах, агрегатах непрерывного действия. Вдуваемый в расплавленный чугун кислород окисляет углерод и примеси, но в конце процесса, когда содержание углерода и примесей понижается, может начаться окисление железа. Оксиды железа переходят в шлак и частично растворяются в стали, делая ее хрупкой.
Для разрушения растворимой закиси железа FeO в расплав вводят раскислители — специальные сплавы марганца, кремния и алюминия с железом (ферросплавы). Входящие в раскислитель Мп, Si и А1 отнимают кислород от оксидов железа, образуя нелетучие продукты, переходящие в шлак. В конце плавки сталь кипит — из нее выделяются растворенные кислород, азот и водород. Введенные раскислители связывают кислород в оксиды, переходящие в шлак, и кипение уменьшается. Раскисление кремнием переводит кипящую сталь в полуспокойную, а совместно с кремнием и алюминием — в спокойную. Кипящая сталь является наиболее хрупкой, пористой и химически неоднородной. Азот и водород удаляют дегазацией (вакуумированием) ванны.